Lithiumchlorid (LiCl) ist ein leicht lösliches, weißes, kristallines Lithiumsalz, das zerfließt und einen salzigen Geschmack hat. Es wird als wenig giftig eingestuft, verursacht aber starke Reizungen und Verätzungen der Augen und Schleimhäute. Lithiumchlorid wird häufig in der Metallurgie, als Trocknungsmittel für Klimaanlagen und als Batterieelektrolyt verwendet .
Seine wässrige Lösung weist eine starke elektrische Leitfähigkeit auf, aber es sollte in einer feuchtigkeitsgeschützten Umgebung gelagert werden, und wegen seiner reizenden Eigenschaften ist bei der Handhabung Vorsicht geboten. In den folgenden Abschnitten werden die grundlegenden Eigenschaften und Anwendungen von Lithiumchlorid unter verschiedenen Aspekten vorgestellt.
Was ist Lithiumchlorid??
Lithiumchlorid ist eine weiße, kristalline Verbindung mit zerfließenden Eigenschaften. Es ist gut löslich in Wasser, Ethanol und Ether und schwach löslich in organischen Lösungsmitteln wie Aceton, Pyridin und flüssigem Ammoniak. Obwohl seine Struktur der von Natriumchlorid ähnelt , handelt es sich bei den chemischen Bindungen in LiCl nicht um typische Ionenbindungen, so dass es sich in einer Vielzahl von organischen Lösungsmitteln auflösen und verschiedene Addukte mit Ethanol, Methanol und Aminen bilden kann. Aufgrund dieser Eigenschaft wird Lithiumchlorid häufig als Medium in Trennverfahren verwendet, um es aus alkalimetallchloriden.
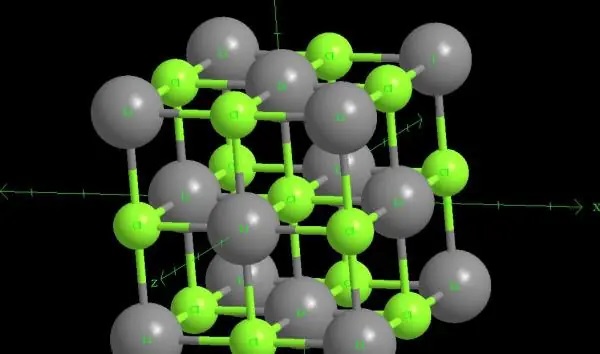
Außerdem hat Lithiumchlorid aufgrund des kleinen Radius des Lithiumions und seiner hohen Hydratationsenergie eine Löslichkeit von bis zu 83 g/100 ml bei 20 °C, die weit über der anderer Chloride der Gruppe liegt. Infolgedessen weist seine wässrige Lösung leicht basische Eigenschaften auf.
Darüber hinaus kann LiCl mit verschiedenen Stoffen reagieren. So reagiert es beispielsweise mit Schwefelsäure unter Bildung von Lithiumsulfat und Chlorwasserstoffgas. An der Luft nimmt Lithiumchlorid leicht Feuchtigkeit auf und verflüssigt sich, weshalb es in einem verschlossenen Behälter gelagert werden muss.
Grundlegende Eigenschaften
| Parameter | Wert |
|---|---|
| Chemische Formel | LiCl |
| Molekulargewicht | 42.39 g/mol |
| Dichte | 2.07 g/ml |
| Schmelzpunkt | 605 °C |
| Siedepunkt | 1380 °C |
| Brechungsindex | 1.381 |
Lithiumchlorid ist gut wasserlöslich, und seine Löslichkeit nimmt mit der Temperatur zu; bei 20 °C können sich etwa 84 g Lithiumchlorid in 100 g Wasser lösen. Seine wässrige Lösung ist neutral und weist eine gute elektrische Leitfähigkeit auf. LiCl besitzt außerdem eine hohe thermische Stabilität und zersetzt sich in trockenem Zustand nicht leicht.
Herstellungsmethoden von Lithiumchlorid
In der industriellen Produktion wird LiCl hauptsächlich aus Lithiumerzen oder Salzlaugen hergestellt . Gängige Verfahren sind die Gewinnung aus Spodumenerz, das zerkleinert, geröstet und mit Salzsäure umgesetzt wird, gefolgt von Verdampfung und Kristallisation, um das Produkt zu erhalten, oder die Herstellung aus Salzsole durch Verdampfung und Trennverfahren. Diese Verfahren umfassen sowohl physikalische als auch chemische Behandlungen und erfordern eine sorgfältige Kontrolle von Temperatur, Konzentration und anderen Parametern.
Einige Reagenzienhersteller stellen wasserfreies LiCl durch Heißfiltration einer auf 100-110 °C eingedampften wässrigen LiCl-Lösung her, wobei ein wasserfreies Salz entsteht. Bei diesem Verfahren wird jedoch durch Erhitzen das Kristallisationswasser entfernt und das LiCl teilweise hydrolysiert, wodurch HCl verloren geht und ein leicht basisches Produkt entsteht. Für die Herstellung von reinem wasserfreiem LiCl sind strengere Methoden erforderlich, z. B. Dehydratisierung unter vermindertem Druck, Miterhitzen mit NH₄Cl und Erhitzen in einem trockenen HCl-Gasstrom auf bis zu 200 °C oder Sprühtrocknung unter sauerstofffreien Bedingungen mit reinem Stickstoff.

Wofür wird Lithiumchlorid verwendet?
Lithiumchlorid wird hauptsächlich in Klimaanlagen, als Flussmittel, Trockenmittel, chemisches Reagenz und bei der Herstellung von Feuerwerkskörpern, Trockenbatterien und metallischem Lithium verwendet.
- Wasserfreies Lithiumchlorid ist ein wichtiger Rohstoff für die Herstellung von metallischem Lithiumes wird hauptsächlich in Elektrolyseverfahren verwendet.
- In der metallurgischen Industrie dient es als Zusatzstoff in der Aluminiumelektrolyse und trägt dazu bei, den Schmelzpunkt zu senken und die Effizienz zu verbessern.
- In Klimaanlagen dienen Lithiumchloridlösungen als Trockenmittel, das die Feuchtigkeit aus der Luft aufnimmt.
- In der Batterieindustrie wird es bei der Herstellung von Lithium-Mangan-Batterieelektrolyten verwendet, um die Ionenleitfähigkeit zu verbessern.
- LiCl wird auch bei der Herstellung von Arzneimitteln und Feuerwerkskörpern verwendet.
- In Labors wird es häufig in der biologischen und chemischen Forschung verwendet.
Zukünftige Entwicklung
Mit dem technologischen Fortschritt können sich die Anwendungen von Lithiumchlorid auf neue Bereiche wie die Energiespeicherung und die Materialwissenschaft ausweiten. Als vielseitige und weit verbreitete Verbindung spielt LiCl sowohl in der Industrie als auch in der Forschung weiterhin eine wichtige Rolle.
